PDF chapter test TRY NOW
சில ஐசோடோப்புகள் கதிரியக்கத் தன்மை
பெற்றுள்ளன ஏன் என்று தெரியுமா?
ஒரு அணுவின் உட்கருவில் உளள நியூட்ரான்களின் எண்ணிக்கை அந்த உட்கருவில் உள்ள புரோட்டான்களின் எண்ணிக்கையை விட அதிகமாகும் போது சில உட்கருக்கள் நிலைப்புத்தன்மை அற்றதாக உள்ளது. இந்த நிலைப்புத்தன்மையற்ற உட்கருக்கள் பிளவுற்று கதிரியக்கத்தை தொடர்ச்சியாக உமிழ்கின்றன. இவை கதிரியக்க ஐசோடோப்புகள் எனப்படுகின்றன.
Example:
\(H^3\) மற்றும் \(C^1{^4}\)
பல தனிமங்கள் ஐசோடோப்புகளைக் பெற்றுள்ளன. அவற்றுள் சில கதிரியக்கத் தன்மை கொண்டவை.
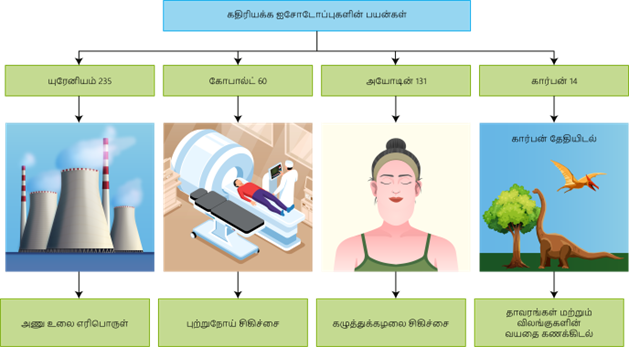
கதிரியக்க ஐசோடோப்புகளின் பயன்கள்:
நாம் உண்ணும் உணவு, சுவாசிக்கும்
காற்று, வாழும் கட்டிடங்கள் என நம்மைச்
சுற்றிலும் குறைந்த அளவில் கதிரியக்கத் தன்மை
கொண்ட பொருட்கள் உள்ளன. இந்த
கதிரியக்கம் எப்போதும் காணப்படும்.
எனவே நம்மைச் சுற்றிலும் அதிக
அளவில் இயற்கையாக குறைந்த கதிரியக்கம்
காணப்படுகிறது. எடுத்துக்காட்டாக நமது உடலில் காணப்படும் பொட்டாசியம் - 40
என்ற கதிரியக்க ஐசோடோப்பு தொடர்ந்து
கதிரியக்கத்தை மிகக் குறைந்த அளவில்
உமிழ்கிறது, இருப்பினும் அவை நம் உடலில் எவ்விதமான பாதிப்பையும்
ஏற்படுத்துவது இல்லை.
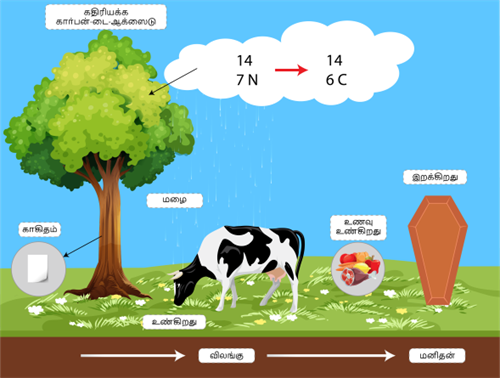
கதிரியிக்க ஐசோடோப்புகளின் பயன்கள்
மேலே உள்ள படம்
கதிரியக்க கார்பன் (\(C^1{^4}\)) நம்மைச் சுற்றிலும் உள்ளன என்பதனைக் காட்டுகிறது. ஆனால் கதிரியிக்க ஐசோடோப்புகளின் சிறப்புப்
பண்புகள் பல்வேறுத்துறைகளில் நமக்குப்
பயன்படுகின்றன.