PDF chapter test TRY NOW
மூலக்கூறுகளை நாம் கீழே கொடுக்கப்பட்டுள்ளவாறு
வகைப்படுத்தலாம்.
ஓரே ஒரு அணுவைக் கொண்டுள்ள மூலக்கூறுகள் ஓரணு மூலக்கூறுகள் எனப்படும்.
Example:
மந்த வாயுக்கள்
இரண்டு அணுக்களைக் கொண்டுள்ள மூலக்கூறுகள் ஈரணு மூலக்கூறுகள் எனப்படும்.
Example:
ஆக்சிஜன், நைட்ரிக் ஆக்ஸைடு மற்றும் ஹைட்ரஜன்.
மூன்று அணுக்களைக் கொண்டுள்ள மூலக்கூறுகள் மூவணு மூலக்கூறுகள் எனப்படும்.
Example:
ஓசோன், சல்பர் டை ஆக்ஸைடு, கார்பன்-டை-ஆக்ஸைடு.
மூன்றுக்கும் மேற்பட்ட அணுக்களைக் கொண்டுள்ள மூலக்கூறுகள் பல் அணு (அ )பல அணு மூலக்கூறுகள் எனப்படும்.
Example:
பாஸ்பேட், சல்பர்.
தனிமத்தின் மூலக்கூறுகள்:
வேதி பிணைப்பினால் பிணைக்கப்பட்ட ஒரு குறிப்பிட்ட எண்ணிக்கையிலான ஒரே வகையான அணுக்களைத் தனிமத்தின் மூலக்கூறுகள் கொண்டுள்ளன.
இரண்டு அணுக்களைக் கொண்ட ஒரே
வகையான தனிமத்தினால் ஆன சில வாயுக்களைக்
கீழே கொடுக்கபட்டுள்ள படத்தில் காணலாம்.
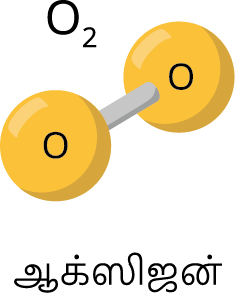
சேர்மங்களின் மூலக்கூறுகள்:
வேதி பிணைப்பினால் பிணைக்கப்பட்ட குறிப்பிட்ட எண்ணிக்கையிலான வேறுபட்ட அணுக்களைத் தனிமத்தின் மூலக்கூறுகள் கொண்டுள்ளன.
உதாரணமாக நீர் மூலக்கூறு மாதிரியைக்
எடுத்துக்கொள்வோம்.
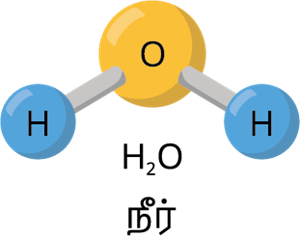
ஒவ்வொரு நீர் மூலக்கூறும் ஒரு ஆக்சிஜன் அணுவினையும், இரண்டு ஹைட்ரஜன் அணுக்களையும் பெற்றுள்ளன. ஆக்சிஜன் மற்றும் ஹைட்ரஜனின் இந்த விகிதமானது திண்மம் , நீர்மம் மற்றும் வாயு என எந்த நிலையில் காணப்பட்டாலும் மாறாததாகக் உள்ளது. இந்தத் தத்துவமானது அனைத்துச் சேர்மங்களின் மூலக்கூறுகளுக்கும் பொருந்துவதாக அமையும்.
