
PUMPA - SMART LEARNING
எங்கள் ஆசிரியர்களுடன் 1-ஆன்-1 ஆலோசனை நேரத்தைப் பெறுங்கள். டாப்பர் ஆவதற்கு நாங்கள் பயிற்சி அளிப்போம்
Book Free Demoவேதியியலில் அணுக்கட்டு எண் என்பது, ஒரு தனிமத்தில் அல்லது சேர்மத்தில் அல்லது பொருளில் அடங்கியுள்ள ஒட்டுமொத்த அணுக்களின் எண்ணிக்கையைக் குறிப்பதாகும்.
ஒரு தனிமத்தினுடைய அணுக்கட்டு
எண்ணை எவ்வாறு கணக்கிடுவது என்பதைக்
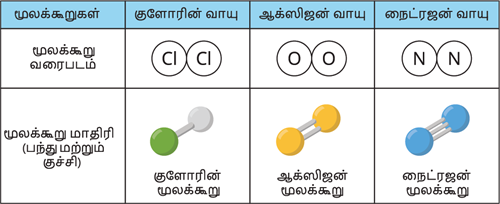
காண்போம். உதாரணமாக, ஆக்சிஜன் ஒரு
ஈரணுமூலக்கூறாகும். அதாவது ஒரு ஆக்சிஜன்
மூலக்கூறில் இரண்டு ஆக்சிஜன் அணுக்கள்
உள்ளன. எனவே ஆக்சிஜனுடைய அணுக்கட்டு
எண் \(2\) ஆகும்.
\(O + O \to O_2\)
(ஆக்சிஜன் அணு + ஆக்சிஜன் அணு → ஆக்சிஜன் மூலக்கூறு)
அதே போல் பாஸ்பரஸ் (P4) மூலக்கூறு நான்கு
அணுக்களைக் கொண்டுள்ளது, சல்பர் (\(S_8\))
மூலக்கூறு எட்டு அணுக்களைக் கொண்டுள்ளது.
ஆகவே அவற்றின் அணுக்கட்டு எண் முறையே
நான்கு மற்றும் எட்டு ஆகும்.
ஒன்றுக்கு அல்லது அதற்கு மேற்பட்ட வெவ்வேறு வகையான
அணுக்களைக் கொண்ட ஒரு மூலக்கூறின்
அணுக்கட்டு எண்ணை அவற்றில் எத்தனை
அணுக்கள் உள்ளதோ அவற்றினைக்
கூட்டுவதன் மூலம் நாம் பெற முடியும்.
உதாரணமாகக் கந்தக அமிலத்தில் (\(H_2SO_4\))
இரண்டு ஹைட்ரஜன் அணுவும், ஒரு சல்பர்
அணுவும் மற்றும் நான்கு ஆக்சிஜன் அணுவும்
உள்ளன. ஆகவே கந்தக அமிலத்தினுடைய
அணுக்கட்டு எண் 2+1+4 = 7 ஆகும்.
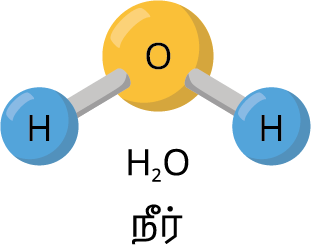
நீர் (\(H_2O\)) மூலக்கூறு இரண்டு ஹைட்ரஜன்
அணுக்கள் மற்றும் ஒரு ஆக்சிஜன் அணுவினால்
ஆனது. ஆகவே நீரின் அணுக்கட்டு எண் மூன்று ஆகும்.
சில தனிமங்களின் அணுக்கட்டு எண்கள்:
தனிமம் | அணுக்கட்டு எண் |
H | \(2\ \) |
Be | \(1\) |
N | \(2\) |
P | \(4\) |
S | \(8\) |
மனித உடலில் உள்ள தனிமங்கள்:
மனித உடலின் நிறையில் ஏறத்தாழ \(99\) சதவிகிதம் நிறையனது ஆறு வேதியியல் தனிமங்களால் மட்டும் ஆனதாகும்.
அவை: ஆக்சிஜன், கார்பன், நைட்ரஜன் கால்சியம் மற்றும் பாஸ்பரஸ், மற்றும் ஐந்து தனிமங்களான பொட்டாசியம், சல்பர், சோடியம், குளோரின் மற்றும் மெக்னீஷியம் போன்ற தனிமங்கள் குறைந்த அளவில் உடலில் கணப்படுகின்றன.
காற்றில் உள்ள தனிமங்கள்:
காற்றானது வாயுக்கலவையின் தொகுப்பாகும். காற்றில் \(99\) சதவிகிதம் நைட்ரஜன் மற்றும் ஆக்ஸிஜன் போன்ற தனிமங்களின் மூலக்கூறுகள் காணப்படுகின்றன.
இவற்றைத் தவிர ஆர்கன் மற்றும் கரியமில வாயு ஆகியவை சிறிய அளவில் உள்ளன.
(நியான், ஹீலியம் மற்றும் மீத்தேன் போன்றவை மிக மிக குறைந்த அளவில் கணப்படுகின்றன).
ஆக்ஸிஜன் ஒரு உயிர் கொடுக்கும் (வாயு) தனிமம் ஆகும்.
ஆக்ஸிஜன் ஒரு உயிர் கொடுக்கும் (வாயு) தனிமம் ஆகும்.